研究成員:博士研究生應夏媛、副研究員林國儀、博士後林芳如(由左至右)Blimp-1 是一個B細胞分化成漿細胞時,誘發出的一個很重要的蛋白。漿細胞在人體免疫機制內的角色,在於負責製造抗體。已知的是,Blimp-1會於細胞分化時,適時作基因的調控,最終方得產生漿細胞;至於這其中的細節,林國儀老師的研究團隊在七月發表於知名的EMBO Reports 期刊後,旋獲A-IMBN摘要報導。幾乎在同時,另外一篇相關的研究,也發表於 Blood 期刊,這些研究,對於人體免疫機制調控的研究,開起了一盞明燈。
研究成員:博士研究生應夏媛、副研究員林國儀、博士後林芳如(由左至右)Blimp-1 是一個B細胞分化成漿細胞時,誘發出的一個很重要的蛋白。漿細胞在人體免疫機制內的角色,在於負責製造抗體。已知的是,Blimp-1會於細胞分化時,適時作基因的調控,最終方得產生漿細胞;至於這其中的細節,林國儀老師的研究團隊在七月發表於知名的EMBO Reports 期刊後,旋獲A-IMBN摘要報導。幾乎在同時,另外一篇相關的研究,也發表於 Blood 期刊,這些研究,對於人體免疫機制調控的研究,開起了一盞明燈。
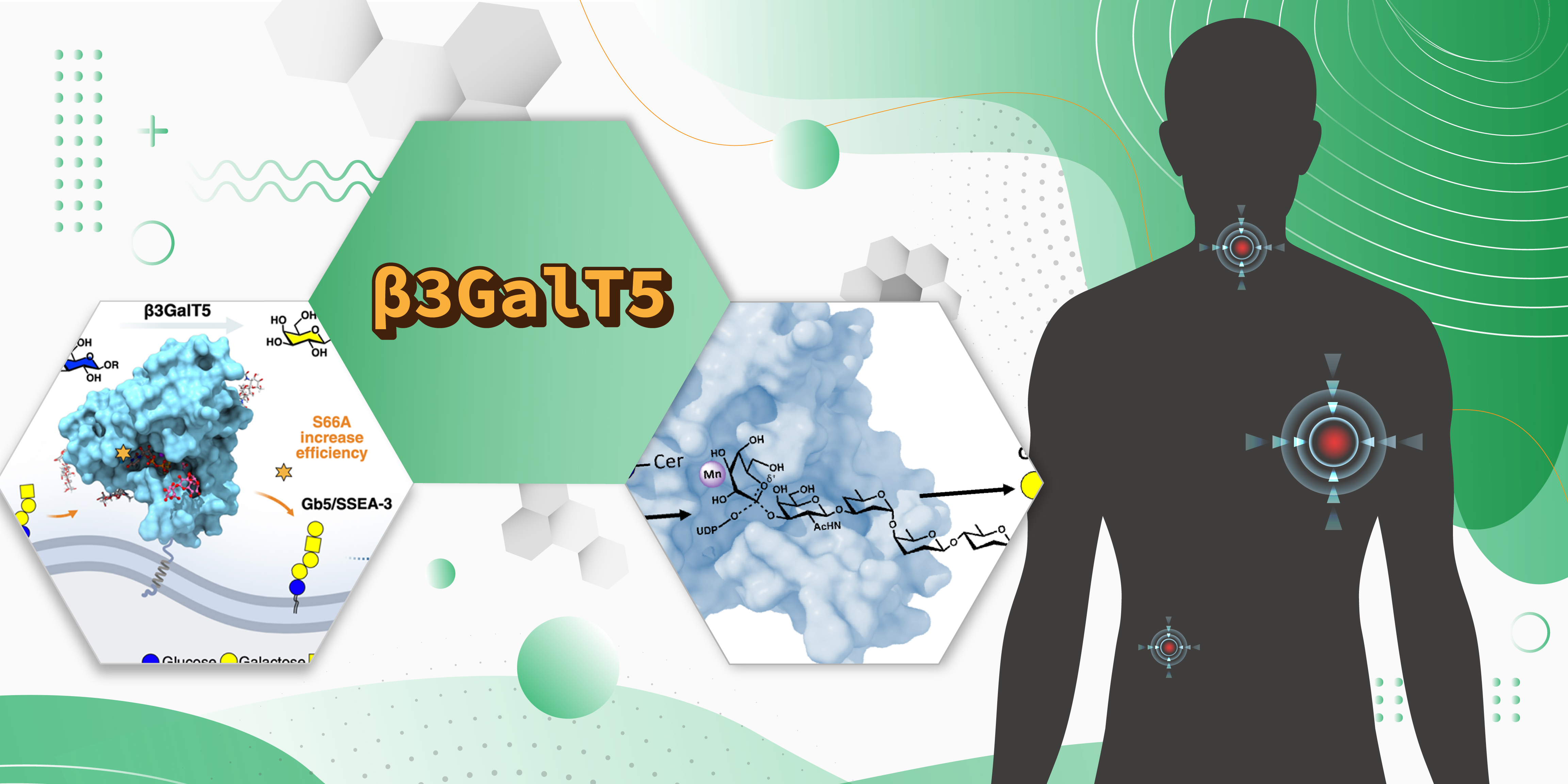
研究團隊發現,Blimp-1 在分化成血漿細胞的過程中,具有統合的角色,首先,它會與PIAS1 分子接觸,接著,經過 Blimp-1表面的K-816點,與細胞內的SUMO分子產生共價結合,然後,再透過與HDAC-2分子的作用,這個B細胞才會分化成為漿細胞。這整個過程就好像一個標準作業流程,然而,SUMO分子扮演關鍵的第三者,研究顯示,倘若剔除SUMO分子與Blimp-1表面的結合,這個製程就完全行不通。
漿細胞是免疫系統根據情報所派出的專一型態的B細胞所分化出來的免疫細胞,漿細胞不會再作分裂,它的任務就在於製造出抗體,就好似一種武器的工廠一樣。當危機解除,漿細胞會停留在人體的骨髓內,等待下一次的任務,也會隨著時間而凋零。然而,漿細胞的壽命似乎並非全都一樣,此外,若漿細胞機能失控,而自行分裂時,就會產生多發性骨髓瘤 (Multiple Myeloma, MM),屬於血液腫瘤科疾病的一種。
 此圖為實驗結果在第二十天時的結果,增加ASK1表現量的實驗鼠內腫瘤細胞已無法以顯影看到,而沒有誘發ASK1表現的實驗鼠則可觀察到到大量腫瘤細胞的顯影。 實驗方式:實驗鼠施打多發性骨髓瘤細胞株後,TRE列為對照組,ASK1列則為用來觀察誘發ASK1於細胞內表現的實驗組,顏色顯示為腫瘤細胞的顯影,顏色愈接近紅色表示腫瘤細胞數目越多。在第六天, ASK1組內,一部份用Dox去誘使實驗鼠體內的ASK1表現量增加(右下),另一部份則無(左下)。針對這些現象,林國儀的實驗室展開另一個棄而不捨的研究,結果,發現了一個極少量但極具關鍵性和毀滅性的分子,ASK1。
此圖為實驗結果在第二十天時的結果,增加ASK1表現量的實驗鼠內腫瘤細胞已無法以顯影看到,而沒有誘發ASK1表現的實驗鼠則可觀察到到大量腫瘤細胞的顯影。 實驗方式:實驗鼠施打多發性骨髓瘤細胞株後,TRE列為對照組,ASK1列則為用來觀察誘發ASK1於細胞內表現的實驗組,顏色顯示為腫瘤細胞的顯影,顏色愈接近紅色表示腫瘤細胞數目越多。在第六天, ASK1組內,一部份用Dox去誘使實驗鼠體內的ASK1表現量增加(右下),另一部份則無(左下)。針對這些現象,林國儀的實驗室展開另一個棄而不捨的研究,結果,發現了一個極少量但極具關鍵性和毀滅性的分子,ASK1。
有趣的是,ASK1 和 Blimp-1在漿細胞內形成一個角力賽,研究顯示,Blimp-1會抑制ASK1的表現,但若Blimp-1轉弱,ASK1的量一旦佔在上風,漿細胞旋即凋亡。
研究團隊取得小鼠正常的漿細胞,以及將人體多發性骨髓瘤患者骨髓內的腫瘤漿細胞移殖到免疫缺失的小鼠身上,再作比對分析,結果,發現了向下調控ASK1的量,會維持小鼠骨髓內的漿細胞;若促使ASK1的表現,則讓漿細胞死亡,亦會讓腫瘤漿細胞死亡。因此,調控ASK1就像使用雙面利刃,可以導致摧毀,也可以用於治療。
研究團隊對於這些發現深感信心,也將更深入的去探討,他們希望這些免疫學上的突破,可以讓將來的疾病治療更有所本。
有關 SUMO 及 Blimp-1 的研究,刊載於 “EMBO reports” 期刊七月份,期刊該期的封面圖,就是Blimp-1如何一路協助B細胞分化成漿細胞的過程以的一個清楚的圖示;此外,A-IMBN 亦於八月八日對於這個研究作摘要報導。
至於 ASK1的研究,以 “ASK1 promotes apoptosis of normal and malignant plasma cells” 為題的論文亦已刊載於八月二日的 BLOOD 期刊。